L’experiment de Miller i Urey
L’experiment de Miller i Urey representa la primera demostració que es poden formar espontàniament molècules orgàniques a partir de substàncies inorgàniques simples en condicions ambientals adequades. Va ser portat a terme 1952 per Stanley Miller i Harold Clayton Urey a la Universitat de Chicago. L’experiment va ser clau per donar suport a la teoria del brou primordial en l’origen de la vida, d’Aleksandr Oparin i J. B. S. Haldane.
Un text MOLT interessant sobre l’origen de la vida
En aquest cas et presentem un text molt més complex però molt més ric que els anteriors. T’aconsello que li facis una llegida.
La aparición de la vida (Descarregar versió en pdf).
En 1953, un estudiante graduado de la Universidad de Chicago, Stanley Miller, cogió dos matraces (uno que contenía un poco de agua para representar el océano primigenio; el otro con una mezcla de metano, amoniaco y sulfuro de hidrógeno en estado gaseoso, que representaba la primitiva atmósfera de la Tierra), los conectó con tubos de goma e introdujo unas chispas eléctricas como sustituto de los rayos. A los pocos días, el agua de los matraces se había puesto verde y amarilla y se había convertido en un sustancioso caldo de aminoácidos, ácidos grasos, azúcares y otros compuestos orgánicos. «Si Dios no lo hizo de este modo —comentó encantado el supervisor de Miller, el premio Nobel Harold Urey—, desperdició una buena opción.»
La prensa de la época hizo que pareciese que lo único que hacía falta era que alguien diese un buen meneo a los matraces para que saliese arrastrándose de ellos la vida. El tiempo ha demostrado que el asunto no era tan simple. A pesar de medio siglo de estudios posteriores, no estamos más cerca hoy de sintetizar la vida que en 1953… Y estamos mucho más lejos de pensar que podemos hacerlo. Hoy los científicos están bastante seguros de que la atmósfera primitiva no se hallaba tan preparada para el desarrollo como el estofado gaseoso de Miller y Urey, que era una mezcla bastante menos reactiva de nitrógeno y dióxido de carbono. La repetición de los experimentos de Miller con estos aportes mucho más completos no ha producido hasta ahora más que un aminoácido bastante primitivo. De todos modos, crear aminoácidos no es en realidad el problema. El problema son las proteínas.
Las proteínas son lo que obtienes cuando logras unir aminoácidos, y necesitamos muchísimas. Nadie lo sabe en realidad, pero puede haber hasta un millón de tipos de proteínas en el cuerpo humano y cada una de ellas es un pequeño milagro. Según todas las leyes de la probabilidad, las proteínas no deberían existir. Para hacer una necesitas agrupar los aminoácidos (a los que estoy obligado por larga tradición a calificar aquí como «los ladrillos de la vida») en un orden determinado, de una forma muy parecida a como se agrupan las letras en un orden determinado para escribir una palabra. El problema es que las palabras del alfabeto de los aminoácidos suelen ser extraordinariamente largas. Para escribir colágeno, el nombre de un tipo frecuente de proteína, necesitas colocar en el orden correcto ocho letras. Para hacer colágeno, hay que colocar 1.055 aminoácidos exactamente en la secuencia correcta. Pero —y es una cuestión obvia pero crucial— no lo haces tú. Se hace solo, espontáneamente, sin dirección; y ahí es donde intervienen las improbabilidades.
Las posibilidades de que una molécula con una secuencia de 1.055 aminoácidos como el colágeno se autoorganice de una forma espontánea son claramente nulas. Sencillamente no sucederá. Para entender hasta qué punto es improbable su existencia, visualiza una máquina tragaperras normal de Las Vegas, pero muy ampliada (hasta los 2.7 metros, para ser exactos), de manera que quepan en ella 1.055 ruedecillas giratorias en vez de las tres o cuatro habituales, y con 20 símbolos en cada rueda (uno por cada aminoácido común).* ¿Cuánto tiempo tendrías que pasarte dándole a la manivela para que llegaran a aparecer en el orden correcto los 1.055 símbolos? Efectivamente, infinito. Aunque redujeses el número de ruedas giratorias a 200, que es en realidad un número más característico de aminoácidos para una proteína, las posibilidades en contra de que apareciesen las 200 en una secuencia prescrita son de 1 entre 10260 (es decir, un 1 seguido de 260 ceros). Esta cifra es por sí sola mayor que el número de todos los átomos del universo. Las proteínas son, en suma, entidades complejas. La hemoglobina sólo tiene 146 aminoácidos, una nadería para criterios proteínicos, pero incluso ella presenta 10190 combinaciones posibles de aminoácidos, que son el motivo de que el químico de la Universidad de Cambridge, Max Perutz, tardase veintitrés años (más o menos una carrera profesional) en desentrañarlas. Que ciertos acontecimientos aleatorios produjesen incluso una sola proteína resultaría algo de asombrosa improbabilidad, comparable al hecho de que un torbellino que pasase por un depósito de chatarra dejase atrás un reactor Jumbo completamente montado, según el pintoresco símil del astrónomo Fred Hoyle.
Sin embargo, estamos hablando de cientos de miles de proteínas, tal vez un millón, únicas cada una de ellas y vitales, por lo que sabemos, cada una para el mantenimiento de un tú sólido y feliz. Y ahí empieza el asunto. Para que una proteína sea útil no sólo debe agrupar aminoácidos en el orden correcto, debe entregarse a una especie de papiroflexia química y plegarse de una forma muy específica. Incluso después de haber alcanzado esa complejidad estructural, una proteína no te servirá de nada si no puede reproducirse, y las proteínas no pueden hacerlo. Por eso necesitas ADN. El ADN es un hacha en lo de la reproducción (puede hacer una copia de sí mismo en cuestión de segundos), pero no es capaz de hacer prácticamente nada más. Así que nos encontramos ante una situación paradójica. Las proteínas no pueden existir sin el ADN y el ADN no vale nada sin las proteínas. ¿Hemos de suponer, pues, que surgieron simultáneamente con el propósito de apoyarse entre sí? Si fue así: ¡puf! Y hay más aún. El ADN, las proteínas y los demás elementos de la vida no podrían prosperar sin algún tipo de membrana que los contenga. Ningún átomo ni molécula ha alcanzado nunca vida independientemente. Desprende cualquier átomo de tu cuerpo y no estará más vivo que un grano de arena. Esos materiales diversos sólo pueden tomar parte en el asombroso baile que llamamos vida cuando se unen en el refugio alimentador de una célula. Sin la célula, no son más que sustancias químicas interesantes. Pero, sin las sustancias químicas, la célula carece también de propósito. Como dice Davies: «Si cada cosa necesita a todas las demás, ¿cómo pudo surgir en principio la comunidad de moléculas?». Es como si los ingredientes de tu cocina se uniesen misteriosamente y se convirtiesen solos en una tarta… pero una tarta que además pudiera dividirse cuando hiciera falta para producir más tartas. No es raro que le llamemos milagro de la vida. Tampoco lo es que apenas hayamos empezado a comprenderlo.
¿Qué es, pues, lo que explica toda esta maravillosa complejidad? Bueno, una posibilidad es que quizá no sea del todo (no del todo) tan maravillosa como parece en principio. Consideremos esas proteínas tan asombrosamente inverosímiles. El prodigio que vemos en su agrupación se debe a que suponemos que aparecieron en escena plenamente formadas. Pero ¿y si las cadenas de proteínas no se agruparon de golpe? ¿Y si en la gran máquina tragaperras de la «creación» pudiesen pararse algunas ruedas, lo mismo que podría conservar un jugador un número de cerezas prometedoras? ¿Y si, dicho de otro modo, las proteínas no hubiesen brotado súbitamente a la existencia, sino que hubiesen evolucionado?
Imagínate que cogieses todos los elementos que componen a un ser humano (carbono, hidrógeno, oxígeno, etcétera) y los pusieses en un recipiente con un poco de agua, lo agitaras con fuerza y saliese una persona. Sería asombroso. Pues bien, eso es lo que vienen a decir Hoyle y otros (incluidos muchos ardorosos creacionistas) cuando afirman que las proteínas se formaron de pronto de forma espontánea. No es posible tal cosa… no pudo ser así. Como explica Richard Dawkins en El relojero ciego, tiene que haber habido algún tipo de proceso de selección acumulativo que permitió agruparse a los aminoácidos. Tal vez se unieron dos o tres aminoácidos con algún objetivo simple y luego, al cabo de un tiempo, se tropezaron con otro pequeño grupo similar y, al hacerlo, «descubrieron» alguna mejora adicional.
Las reacciones químicas del tipo de las que se asocian con la vida son en realidad algo común y corriente. Tal vez no podamos prepararlas en un laboratorio como Stanley Miller y Harold Urey, pero el universo lo hace con bastante frecuencia. Muchas moléculas de la naturaleza se unen para formar largas cadenas denominadas polímeros. Los azúcares se agrupan constantemente para formar almidones. Los cristales pueden hacer muchas cosas parecidas a la vida: reproducirse, reaccionar a los estímulos ambientales, adoptar una complejidad pautada… Nunca han alcanzado la vida misma, por supuesto, pero demuestran de forma insistente que la complejidad es un hecho natural, espontáneo y absolutamente fiable. Puede haber o no mucha vida en el universo en su conjunto, pero lo que no falta es automontaje ordenado, en todas las cosas, desde la pasmosa simetría de los copos de nieve hasta los hermosos anillos de Saturno.
Tan poderosa es esta tendencia natural a la agrupación que muchos científicos creen que la vida puede ser más inevitable de lo que pensamos… que es, en palabras del bioquímico y premio Nobel belga Christian de Duve, «una manifestación obligatoria de la materia, obligada a surgir siempre que se dan las condiciones apropiadas». De Duve consideraba probable que se diesen esas condiciones un millón de veces en cada galaxia.
Desde luego no hay nada demasiado exótico en las sustancias químicas que nos animan. Si quisieras crear otra criatura viva, ya sea una perca dorada, un cogollo de lechuga o un ser humano, sólo necesitarías cuatro elementos principales: carbono, hidrógeno, oxígeno y nitrógeno, más pequeñas cantidades de algunos más, principalmente azufre, fósforo, calcio y hierro. Dispón esos elementos unidos en tres docenas de combinaciones o así para formar más azúcares, ácidos y otros compuestos básicos y podrás construir cualquier ser vivo. Como dice Dawkins: «Las sustancias de las que están hechas las cosas vivas no tienen nada de especial. Las cosas vivas son colecciones de moléculas, como todo lo demás».
El balance final es que la vida es asombrosa y gratificante, tal vez hasta milagrosa, pero de ningún modo imposible… como atestiguamos una y otra vez con nuestra humilde existencia. Muchos de los pequeños detalles de los comienzos de la vida siguen siendo, claro, bastante imponderables. Todos los escenarios sobre los que hayas podido leer relacionados con las condiciones necesarias para la vida incluyen agua (desde el «cálido charquito» donde suponía Darwin que se inició la vida, a las burbujeantes chimeneas submarinas que son ahora las candidatas más probables para el inicio de la vida), pero aquí se pasa por alto el hecho de que, para convertir monómeros en polímeros (es decir, para empezar a crear proteínas), hace falta un tipo de reacción que se denomina en biología «enlaces de deshidratación». Como dice un destacado texto de esa disciplina, tal vez con sólo una leve sombra de desasosiego:” «Los investigadores coinciden en que esas reacciones no habrían sido energéticamente favorables en el mar primitivo, o en realidad en ningún medio acuoso, debido a la ley de acción de masas». Es algo muy parecido a echar azúcar en un vaso de agua y que se convierta en un cubo. No debería suceder, pero el hecho es que sucede en la naturaleza. Los procesos químicos concretos de todo esto son un poco crípticos para lo que nos proponemos aquí, pero hasta con saber que, si humedeces monómeros, no se convierten en polímeros… salvo cuando crearon la vida en la Tierra. Cómo y por qué sucedió eso entonces y no sucedió otra cosa es uno de los grandes interrogantes de la biología.
Una de las mayores sorpresas de las ciencias de la Tierra en las décadas recientes fue precisamente el descubrimiento de cuándo surgió la vida en la historia de la Tierra. Todavía bien entrados los años cincuenta se creía que la vida tenía menos de 600 millones de años de antigüedad: En la década de los setenta, unas cuantas almas intrépidas creían ya que tal vez se remontase a 2.500 millones de años. Pero la cifra actual de 3.850 millones de años sitúa el origen de la vida en un pasado de clamorosa antigüedad. La superficie de la Tierra no empezó a solidificarse hasta hace unos 3.900 millones de años.
«Sólo podemos deducir de esa rapidez que para las bacterias no es “difícil” evolucionar en planetas que reúnan las condiciones adecuadas», opinaba Stephen Jay Gould en el New York Times en 1996. 0, como él mismo decía en otro lugar, es difícil eludir la conclusión de que «la vida, al surgir tan pronto como podía hacerlo, estaba químicamente destinada a ser ».
La vida afloró tan deprisa, en realidad, que algunas autoridades en la materia piensan que tuvo que haber contado con alguna ayuda… tal vez bastante ayuda. La idea de que la vida terrestre pudiese haber llegado del espacio tiene una historia sorprendentemente larga e incluso distinguida en ocasiones. El gran lord Kelvin planteó la posibilidad, en 1871, en un congreso de la Asociación Británica para el Progreso de la Ciencia, cuando dijo que «los gérmenes de la vida pudo haberlos traído a la Tierra algún meteorito». Pero esto quedó como poco más que una idea marginal hasta que, un domingo de septiembre de 1969, una serie de explosiones sónicas y la visión de una bola de fuego cruzando el cielo de este a oeste sobresaltó a decenas de miles de australianos.’? La bola de fuego hizo un extraño sonido chisporroteante al pasar y dejó tras ella un olor que a algunos les pareció como a alcohol metilado y otros se limitaron a calificar de espantoso.
La bola de fuego estalló encima de Murchison, una población de seiscientos habitantes situada en Goulburn Valley, al norte de Melbourne, y cayó en una lluvia de fragmentos, algunos de los cuales pesaban más de cinco kilos. Afortunadamente no hicieron daño a nadie. El meteorito era de un tipo raro, conocido como condrita carbonosa, y la gente del pueblo recogió y guardó diligentemente unos 90 kilos de él. El momento no podría haber sido más oportuno. Menos de dos meses antes, habían regresado a la Tierra astronautas del Apolo 11 con un saco lleno de rocas lunares, así que los laboratorios del mundo se estaban preparando para recibir rocas de origen extraterrestre —estaban clamando, en realidad, por ellas.
Se descubrió que el meteorito de Murchison tenía 4.500 millones de años de antigüedad y estaba salpicado de aminoácidos, 74 tipos en total, ocho de ellos involucrados en la formación de las proteínas terrestres. A finales de 2001, más de treinta años después de que cayese, el equipo del Centro de Investigación Ames de California comunicó que la roca de Murchison contenía también cadenas complejas de azúcares llamados poliolos, que no se habían encontrado antes fuera de la Tierra.
Desde 1960 se han cruzado en el camino de la Tierra unas cuantas condritas carbonosas más (una que cayó cerca del lago Tagish en el Yukón canadiense en enero de 2000 resultó visible en grandes sectores de Norteamérica) y han confirmado asimismo que el universo es en realidad rico en compuestos orgánicos. Hoy se cree que un 25% de las moléculas del cometa Halley son moléculas orgánicas. Si un número suficiente de ellas aterriza en un lugar apropiado (la Tierra, por ejemplo), tendrás los elementos básicos necesarios para la vida.
Hay dos problemas relacionados con las ideas de la panespermia, que es como se conocen las teorías del origen extraterrestre de la vida. El primero es que no aclara ninguno de los interrogantes relacionados con cómo surgió la vida; se limita a desplazar la responsabilidad del asunto a otro lugar. El otro es que la panespermia tiende a veces a provocar incluso en sus partidarios más respetables grados de especulación que pueden, sin duda alguna, calificarse de imprudentes. Francis Crick, codescubridor de la estructura del ADN, y su colega Leslie Orgel han postulado que la Tierra fue «deliberadamente sembrada con vida por alienígenas inteligentes», una idea que para Gribbin «se halla en el límite mismo de la respetabilidad científica»… o, dicho de otro modo, una idea que se consideraría descabellada y lunática si no lo expusiese alguien galardonado con el premio Nobel. Fred Hoyle y su colega Chandra Wickramasinghe minaron aún más el entusiasmo por la panespermia sugiriendo, como se indicó en el capítulo 3, que el espacio exterior nos trajo no sólo vida sino también muchas enfermedades como la gripe y la peste bubónica, ideas que fueron fácilmente refutadas por los bioquímicos.
Fuese lo que fuese lo que impulsó a la vida a iniciar su andadura, sucedió sólo una vez. Éste es el hecho más extraordinario de la biología, tal vez el hecho más extraordinario que conocemos. Todo lo que ha vivido, planta o animal, tuvo su inicio a partir del mismo tirón primordial. En un determinado punto de un pasado inconcebiblemente lejano, cierta bolsita de sustancias químicas se abrió paso hacia la vida. Absorbió algunos nutrientes, palpitó suavemente, tuvo una breve existencia. Todo eso pudo haber sucedido antes, tal vez muchas veces. Pero este paquete ancestral hizo algo adicional y extraordinario: se dividió y produjo un heredero. Una pequeña masa de material genético pasó de una entidad viva a otra, y nunca ha dejado de moverse desde entonces.
Fue el momento de la creación para todos nosotros. Los biólogos le llaman a veces el Gran Nacimiento.
«Adonde quiera que vayas en el mundo, cualquier animal, planta, bicho o gota que veas utilizará el mismo diccionario y conocerá el mismo código. Toda la vida es una», dice Matt Ridley. Somos todos el resultado de un solo truco genético transmitido de generación en generación a lo largo de casi 4.000 millones de años, hasta el punto de que puedes coger un fragmento de instrucción genética humana y añadirlo a una célula de levadura defectuosa, y la célula de levadura lo pondrá a trabajar como si fuera suyo. En un sentido muy real, es suyo. El alba de la vida (o algo muy parecido) se halla en una estantería de la oficina de una geoquímica isotópica llamada Victoria Bennett, del edificio de Ciencias de la Tierra de la Universidad Nacional Australiana de Camberra. La señora Bennett, que es estadounidense, llegó de California a esa universidad con un contrato de dos años en 1989 y lleva allí desde entonces. Cuando la visité, a finales de 2001, me pasó un trozo de roca no demasiado grande, compuesto de finas vetas alternadas de cuarzo blanco y un material verde grisáceo llamado clinopiroxeno. La roca procedía de la isla de Akilia, en Groenlandia, donde se encontraron rocas excepcionalmente antiguas en 1997. Las rocas tienen 3.850 millones de años y son los sedimentos marinos más antiguos que se han encontrado hasta el momento.
—No podemos estar seguros de que lo que tienes en la mano haya contenido alguna vez organismos vivos- porque, para saberlo, habría que pulverizarlo —me explicó Bennett—. Pero procede del mismo yacimiento donde se excavó el testimonio de vida más antiguo que se conoce, así que lo más probable es que hubiese vida en él.
Tampoco encontrarías microbios fosilizados, por mucho que buscases. Desgraciadamente, cualquier organismo simple hubiera desaparecido calcinado en los procesos que convirtieron el cieno del océano en piedra. Lo que veríamos, en lugar de eso, si machacásemos la piedra y examinásemos sus restos al microscopio, serían residuos químicos que pudiesen haber dejado atrás los organismos: isótopos de carbono y un tipo de fosfato llamado apatito, que proporcionan juntos un testimonio firme de que la roca contuvo en tiempos colonias de seres vivos.
—Sólo podríamos hacer conjeturas sobre el aspecto que pudo haber tenido el organismo — dijo Bennet—. Probablemente fuese todo lo elemental que puede serlo la vida… pero aun así era vida. Vivía. Se propagaba. Y acabó conduciendo hasta nosotros.
Si te dedicas a rocas muy antiguas, y es indudable que la señora Bennett está dedicada a eso, hace mucho que la Universidad Nacional Australiana es un lugar excelente para trabajar. Eso se debe principalmente al ingenio de un hombre llamado Bill Compston, que ya está jubilado pero que, en la década de los setenta, construyó la primera microsonda iónica sensible de alta resolución, o SHRIMP (es decir, CAMARÓN), que es como se la conoce más afectuosamente por sus iniciales en inglés —Sensitive High Resolution Ion Micro Probe— de microsonido electrónico de alta resolución sensible al ión. Se trata de una máquina que mide la tasa de desintegración del uranio en unos pequeños minerales llamados zircones. Los zircones aparecen en la mayoría de las rocas, aunque no en los basaltos, y son extremadamente duraderos, ya que sobreviven a todos los procesos naturales salvo la subducción. La mayor parte de la corteza de la Tierra ha vuelto a deslizarse en el interior en algún momento, pero los geólogos, sólo esporádicamente (en Australia Occidental y en Groenlandia, por ejemplo) han encontrado afloramientos de rocas que hayan permanecido siempre en la superficie.
La máquina de Compston permitió que se fecharan esas rocas con una precisión sin paralelo. El prototipo del SHRIMP se construyó y torneó en los propios talleres del Departamento de Ciencias de la Tierra, y parecía una cosa hecha con piezas sobrantes, pero funcionaba magníficamente. En su primera prueba oficial, en 1982, fechó la cosa más vieja que se había encontrado hasta entonces, una roca de Australia Occidental de 4.300 millones de años de antigüedad.
—Causó mucho revuelo en la época —me contó Bennett— encontrar tan deprisa algo tan importante con una nueva tecnología.
Me guió pasillo abajo para que viese el modelo actual, el SHRIMP II. Era un aparato de acero inoxidable grande y sólido, de unos 3,5 metros de largo por 1,5 metros de altura, y tan sólidamente
construido como una sonda abisal. En una consola que había frente a él, y pendiente de las hileras de cifras en constante cambio de una pantalla, había un hombre llamado Bob, de la Universidad de Canterbury, Nueva Zelanda. Llevaba allí desde las cuatro de la mañana, me explicó. Eran ya las nueve y disponía de la máquina hasta el mediodía. SHRIMP II funciona las veinticuatro horas del día; son muchas las rocas que hay que fechar. Si preguntas a un par de geoquímicos cómo funciona un aparato así, empezará a hablarte de abundancias isotópicas y de niveles de ionización con un entusiasmo que resulta simpático pero insondable. El resumen de todo ello era, sin embargo, que la máquina es capaz, bombardeando una muestra de roca con corrientes de átomos cargados, de detectar diferencias sutiles en las cantidades de plomo y uranio de las muestras de zircón, pudiendo deducirse a través de ellas con exactitud la edad de las rocas. Bob me explicó que se tarda diecisiete minutos en analizar un zircón y que hay que analizar docenas en cada roca para conseguir una datación fiable. El proceso parece exigir en la práctica el mismo nivel de actividad dispersa, y aproximadamente el mismo estímulo, que un viaje a la lavandería. Pero Bob parecía muy feliz; claro que en Nueva Zelanda la gente suele parecerlo.
El Departamento de Ciencias de la Tierra era una extraña combinación, en parte oficina, enparte laboratorio, en parte depósito de maquinaria.
—Antes fabricábamos todo aquí —dijo—. Teníamos incluso un soplador de vidrio, pero se jubiló. De todos modos, aún tenemos dos machacadores de piedras a jornada completa. Percibió mi expresión de leve sorpresa.
—Tenemos que analizar muchísimas piedras. Y hay que prepararlas con mucho cuidado. Tienes que asegurarte de que no hay ninguna contaminación de muestras anteriores… que no queda polvo ni nada. Es un proceso muy meticuloso.
Me enseñó las máquinas de triturar rocas, que eran realmente impolutas, aunque los trituradores parecían haberse ido a tomar un café. Al lado de las máquinas había grandes cajas que contenían piedras de todos los tamaños y las formas. Era verdad, sin duda, que analizaban muchísimas piedras en la Universidad Nacional Australiana.
Cuando volvimos al despacho de Bennett, después de nuestro recorrido me fijé en que había colgado en la pared un cartel que mostraba una interpretación pintorescamente imaginativa de la Tierra tal como podría haber sido hace 3.500 millones de años, justo cuando empezaba a iniciarse la vida, en el antiguo periodo conocido por la ciencia de la Tierra como Arcaico. En el cartel se veía un paisaje alienígena de volcanes inmensos y muy activos, así como un mar brumoso de color cobrizo bajo un cielo de un rojo chillón. En primer plano se veían los bajíos llenos de estromatolitos, una especie de roca bacteriana. No parecía un lugar muy prometedor para crear y sustentar vida. Le pregunté si la representación era veraz.
—Bueno, hay una escuela de pensamiento que sostiene que en realidad hacía frío entonces porque el Sol era mucho más débil. (Más tarde me enteré de que los biólogos, cuando se ponen jocosos, se refieren a esto como «el problema del restaurante chino »… porque teníamos un dim sun. *)
Sin atmósfera, los rayos ultravioleta del Sol, incluso de un Sol débil, habrían tendido a descomponer cualquier enlace incipiente que estableciesen las moléculas. Y ahí tienes, sin embargo —digo señalando los estromatolitos—, organismos casi en la superficie. Es un rompecabezas.
—Así que no sabemos cómo era el mundo entonces…
—Mmmm —asintió cavilosamente.
—De todos modos, no parece muy propicio para la vida. Pero tuvo que haber —dijo con un cabeceo amistoso— algo que fuese propicio para la vida. Si no, no estaríamos aquí.
Para nosotros no habría sido un medio propicio, desde luego. Si tuvieses que salir de una máquina del tiempo en aquel antiguo mundo del periodo Arcaico, volverías a meterte corriendo en la máquina, porque no había más oxígeno para respirar en la Tierra del que hay hoy en Marte. Todo estaba lleno además de vapores nocivos de ácido clorhídrico y de ácido sulfúrico lo suficientemente potentes para corroer la ropa y quemar la piel. No se habrían podido contemplar además las vistas limpias y luminosas que aparecían en el cartel del despacho de Victoria Bennett. El caldo químico que era la atmósfera entonces habría impedido que llegase mucha luz del Sol a la superficie de la Tierra. Lo poco que pudieses ver estaría brevemente iluminado por relumbrantes y frecuentes fogonazos de relámpagos. En resumen, era la Tierra, pero una Tierra que no identificaríamos como nuestra.
En el mundo del periodo Arcaico había pocos aniversarios y estaban muy espaciados. Durante 2.000 millones de años, las únicas formas de vida eran organismos bacterianos. Vivían, se reproducían, pululaban, pero no mostraban ninguna inclinación especial a pasar a otro nivel de existencia más interesante. En un momento determinado de los primeros 1.000 millones de años, las cianobacterias, o algas verdeazuladas, aprendieron a aprovechar un recurso al que había libre acceso: el hidrógeno que existe en el agua en abundancia espectacular. Absorbían moléculas de agua, se zampaban el hidrógeno y liberaban el oxígeno como desecho, inventando así la fotosíntesis. Como dicen Margulis y Sagan, la fotosíntesis es «indudablemente la innovación metabólica más importante de la historia de la vida en el planeta» y no la inventaron las plantas, sino las bacterias.
Al proliferar las cianobacterias, el mundo empezó a llenarse de O2, para consternación de aquellos organismos para los que era venenoso… Que en aquellos tiempos eran todos. En un mundo anaeróbico (o que no utiliza oxígeno), el oxígeno es extremadamente venenoso. Nuestros glóbulos blancos usan, en realidad, el oxígeno para matar las bacterias invasoras. Que el oxígeno sea fundamentalmente tóxico suele constituir una sorpresa para los que lo encontramos tan grato para nuestro bienestar, pero eso se debe únicamente a que hemos evolucionado para poder aprovecharlo. Para otros seres es aterrador. Es lo que vuelve rancia la manteca y cubre de herrumbre el hierro. Nosotros, incluso, podemos tolerarlo sólo hasta cierto punto. El nivel de oxígeno de nuestras células es sólo aproximadamente un décimo del que existe en la atmósfera. Los nuevos organismos que utilizaban oxígeno tenían dos ventajas. El oxígeno era una forma más eficiente de producir energía y acababa además con organismos competidores. Algunos se retiraron al cenagoso mundo anaeróbico de pantanos y lechos de lagos. Otros hicieron lo mismo, pero más tarde (mucho más tarde) migraron a los tractos digestivos de seres como tú y como yo.
Un buen número de estas entidades primigenias está vivo dentro de tu cuerpo en este momento, ayudando a la digestión de lo que comes, pero rechazando hasta el más leve soplo de O2. Un número incontable más de ellas no consiguió adaptarse y pereció.
Las cianobacterias fueron un éxito fugitivo. Al principio, el oxígeno extra que produjeron no se acumuló en la atmósfera, sino que se combinó con hierro para formar óxidos férricos, que se hundieron hasta el fondo de los mares primitivos. Durante millones de años, el mundo literalmente se oxidó, un fenómeno del que son vívido testimonio los depósitos ribeteados de hierro que proporcionan hoy una parte tan importante del mineral de hierro. Durante muchas decenas de millones de años no sucedió mucho más que esto. Si retrocedieses ahora hasta aquel primitivo mundo del Proterozoico, no hallarías muchos signos prometedores en la Tierra para la vida futura. Tal vez encontrases de cuando en cuando una película de suciedad viva o una capa de marrones y verdes brillantes en rocas de la costa, pero por lo demás la vida se mantendría invisible.
Sin embargo, hace unos 3.500 millones de años se hizo patente algo más notorio. Donde el mar era poco profundo empezaron a aparecer estructuras visibles. Cuando las cianobacterias pasaban por sus rutinas químicas se hacían un poquito pegajosas, y esa pegajosidad atrapaba micropartículas de polvo y arena que se unían para formar estructuras un poco extrañas pero sólidas (los estromatolitos representados en las aguas poco profundas del mar del cartel del despacho de Victoria Bennett). Los estromatolitos tenían diversas formas y tamaños. Parecían unas veces enormes coliflores, a veces colchones esponjosos (estromatolitos viene de la palabra griega que significa colchón); otras veces tenían forma de columnas, se elevaban decenas de metros por encima de la superficie del agua (llegaban a veces a los 100 metros). Eran en todas sus manifestaciones una especie de roca viviente y constituyeron la primera empresa cooperativa del mundo, viviendo algunas variedades justo en la superficie, y otras justo por debajo de ella, y aprovechando cada una las condiciones creadas por la otra. El mundo tuvo así su primer ecosistema.
Los científicos conocían los estromatolitos por formaciones fósiles, pero en 1961 se llevaron una auténtica sorpresa al descubrirse una comunidad de estromatolitos vivos en la bahía Shark, en la remota costa del noroeste de Australia. Fue un descubrimiento de lo más inesperado… tan inesperado, en realidad, que los científicos tardaron varios años en darse cuenta cabal de lo que habían encontrado. Hoy, sin embargo, la bahía Shark es una atracción turística… o lo es al menos en la medida en que puede llegar a ser una atracción turística un lugar que queda a cientos de kilómetros del resto del mundo y a docenas de kilómetros de algún sitio en el que se pueda estar. Se han construido paseos marítimos entarimados en la bahía para que los visitantes puedan caminar sobre el agua y contemplar a gusto los estromatolitos, que están allí respirando muy tranquilos bajo la superficie. Son grises y sin brillo y parecen, como he dicho ya en un libro anterior, boñigas muy grandes. Pero resulta curioso y turbador considerar que estás contemplando restos vivos de la Tierra tal como era hace 3.500 millones de años. Como ha dicho Richard Fortey: «Esto es viajar de verdad en el tiempo y, si el mundo estuviese conectado con sus auténticas maravillas, este espectáculo sería tan bien conocido como las pirámides de Gizeh». Aunque tú nunca lo dirías, esas rocas mates están llenas de vida: en cada metro cuadrado de roca se calcula que hay (es un cálculo estimativo, claro) 3.000 millones de organismos individuales. A veces, cuando miras detenidamente, llegas a ver pequeños anillos de burbujas que ascienden a la superficie que es el oxígeno del que se están deshaciendo. Estos minúsculos procesos elevaron el nivel de oxígeno en la atmósfera de la Tierra al 20%, preparando el camino para el capítulo siguiente, y más complejo, de la historia de la vida.
Se ha llegado a decir que las cianobacterias de la bahía Shark tal vez sean los organismos de más lenta evolución de la Tierra, y es indudable que se cuentan hoy entre los más raros. Después de preparar el camino para formas de vida más complejas, los devoraron borrándolos de la existencia precisamente esos organismos cuya existencia habían hecho ellos mismos posible. (Perviven en bahía Shark porque las aguas son demasiado saladas para las criaturas que se los comerían.)
Una razón de que la vida tardase tanto en hacerse compleja fue que el mundo tuvo que esperar a que los organismos más simples hubiesen oxigenado lo suficiente la atmósfera. «Los animales no podían reunir la energía suficiente para trabajar», como ha dicho Fortey. Hicieron falta unos dos mil millones de años, aproximadamente el 40% de la historia de la Tierra, para que los niveles de oxígeno alcanzasen más o menos los niveles modernos de concentración en la atmósfera. Pero una vez dispuesto el escenario, y al parecer de forma completamente súbita, surgió un tipo de célula del todo nuevo… una célula que contenía un núcleo y otros cuerpos pequeños denominados colectivamente organelos (que significa en griego «instrumentitos»). Se cree que se inició el proceso cuando alguna bacteria equivocada o aventurera invadió otra o fue capturada por ella y resultó que eso les pareció bien a ambas. La bacteria cautiva se cree que se convirtió en una mitocondria. Esta invasión mitocóndrica (o acontecimiento endosimbiótico, como les gusta denominarlo a los biólogos) hizo posible la vida compleja. (Una invasión similar produjo en las plantas los cloroplastos, que las permiten fotosintetizar.)
Las mitocondrias manipulan el oxígeno de un modo que libera energía de los alimentos. Sin este ingenioso truco auxiliador, la vida en la Tierra no sería hoy más que un fango de simples microbios. Las mitocondrias son muy pequeñas (podrías meter mil millones de ellas en el espacio que ocupa un grano de arena), pero también muy voraces. Casi todos los nutrientes que absorbes son para alimentarlas.
No podríamos vivir dos minutos sin ellas, pero incluso después de mil millones de años las mitocondrias se comportan como si las cosas pudiesen no llegar a ir bien entre nosotros. Conservan su propio ADN, su ARN y sus ribosomas. Se reproducen a un ritmo diferente que sus células anfitrionas. Parecen bacterias, se dividen como bacterias y reaccionan a veces a los antibióticos como lo hacen las bacterias. Ni siquiera hablan el mismo lenguaje genético que la célula en la que viven. En suma, no han deshecho las maletas. Es como tener un extraño en tu casa, pero uno que llevase allí mil millones de años.
El nuevo tipo de células se conoce como eucariota (que significa «verdaderamente nucleadas»), a diferencia del viejo tipo, que se conocen como procariotas ( «prenucleadas» ), y parecen haber llegado súbitamente al registro fósil. Las eucariotas más viejas que se conocen, llamadas Grypania, se descubrieron en sedimentos de hierro de Michigan en 1992. Esos fósiles sólo se han encontrado una vez y luego no se vuelve a tener noticia de ellos en 500 millones de años.
La Tierra había dado su primer paso para convertirse en un planeta verdaderamente interesante. Las viejas células procariotas, comparadas con las nuevas eucariotas, eran poco más que «bolsas de sustancias químicas por utilizar la expresión del geólogo inglés Stephen Drury.
Las eucariotas eran mayores (llegarían a ser hasta 10.000 veces más grandes) que sus primas más sencillas, y podían contener hasta mil veces más ADN. De forma gradual, gracias a estos avances, la vida fue haciéndose más compleja y creó dos tipos de organismos: los que expelen oxígeno (como las plantas) y los que lo absorben (como los animales).
A los organismos eucariotas unicelulares se los llamó en tiempos protozoos («preanimales»), pero ese término se desechó progresivamente. Hoy el término común para designarlos es el de protistas. Comparadas con las bacterias, esas nuevas protistas eran unas maravillas de diseño y de refinamiento. La simple ameba, sólo una célula grande y sin más ambiciones que existir, contiene 400 millones de bites de información genética en su ADN… lo suficiente, según Carl Sagan, para llenar 80 libros de quinientas páginas.
Al final, las células eucariotas aprendieron un truco aún más singular. Costó mucho tiempo (unos mil millones de años), pero estuvo muy bien cuando consiguieron dominarlo. Aprendieron a agruparse en seres pluricelulares complejos. Gracias a esta innovación fueron posibles entidades grandes, visibles y complejas como nosotros. El planeta Tierra estaba listo para pasar a su siguiente y ambiciosa fase.
Pero antes de que nos emocionemos demasiado con eso, es conveniente recordar que el mundo, como estamos a punto de ver, pertenece aún a «lo muy pequeño».
*Existen, en realidad, 22 aminoácidos naturales conocidos en la Tierra. Y puede haber más esperando que los descubramos. Pero sólo son necesarios 20 para producirnos y para producir la mayoría de los demás seres vivos. El que hace el número 22, llamado pirrolisina, fue descubierto el año 2002 por los investigadores de la Universidad Estatal de Ohio. Sólo se encuentra en un tipo de arquea (forma de vida básica que analizaremos un poco más adelante) denominada Methanosarcina barkeri. (N. del A.)
* Dim sun es la transcripción aproximada de un aperitivo cantonés, que en chino significa «toca el corazón», pero que en inglés significa «Sol tenue».
Documental sobre Darwin i l’evolució
A continuació visionarem un documental sobre Darwin i la seva teoria. És molt interessant i dóna una visió molt didàctica de l’evolució. Un cop vist cal respondre les següents preguntes. COMPTE. No el puc penjar on line de manera que seria bo que abans féssiu un cop d’ull a les preguntes que trobareu aquí.
Breu presentació sobre evolució humana
A la recerca del primer europeu – DOCUMENTAL
Després de mirar smb atenció aquest documental respon les preguntes que trobaràs en aquest document.
Per reflexionar…
A continuació tens diversos fragments de dos articles de David Bueno (catedràtic de genètica de la UB).
TRIA LA TEVA PARELLA
 Una de les preocupacions de moltes persones és trobar la seva parella ideal, tant per avenir-se com a persones com, potser de manera més inconscient, per tenir fills sans. En aquest sentit, no es tracta de buscar una certa “qualitat genètica” en la parella, sinó que la combinació de les variants gèniques dels dos progenitors sigui prou satisfactòria perquè els fills, en heretar-les siguin sans.
Una de les preocupacions de moltes persones és trobar la seva parella ideal, tant per avenir-se com a persones com, potser de manera més inconscient, per tenir fills sans. En aquest sentit, no es tracta de buscar una certa “qualitat genètica” en la parella, sinó que la combinació de les variants gèniques dels dos progenitors sigui prou satisfactòria perquè els fills, en heretar-les siguin sans.
Ja fa unes quantes dècades que van aparèixer les agències matrimonials, que cercaven la parella “ideal” per a cada persona segons uns tests psicològics. Ara, però, l’aplicació dels coneixements genètics i de les tècniques d’anàlisi de material hereditari han fet possible realitzar tests genètics amb aquesta finalitat. El 2007 va néixer la primera empresa als Estats Units. La idea és molt simple: analitzar determinats gens implicats en el funcionament del sistema immunlògic adequat per als descendents, però en realitat va molt més enllà, perquè aquests gens també participen en els processos instintius d’atracció sexual, entre els quals hi ha l’olor corporal pròpia de cada persona.
En certa manera és el que instintivament fem quan cerquem parella: avaluar la compatibilitat genètica en funció, entre altres característiques, de la seva olor. Ja fa temps que se sap que aquesta és una de les barreres biològiques contra un excés de consanguinitat. La consanguinitat representa un problema biològic, atès que augmenta molt les possibilitats que s’ajuntin en una mateixa persona dues variants gèniques idèntiques que no siguin plenament funcionals, la qual cosa provocaria una malaltia genètica.
Doncs bé, hi ha estudis que indiquen que hom se sent atret per aquelles persones que tenen variants gèniques diferents de les seves, una manera instintiva d’evitar la consanguinitat, i que ho avaluem mitjançant l’olor corporal.
DONES FIDELS I HOMES ADÚLTERS
 Tradicionalment, els humans ens hem comportat de forma monògama quant a la cura de la descendència, la qual cosa no exclou que durant l’etapa reproductora una femella es pugui aparellar amb diversos mascles i un mascle amb diverses femelles. Tanmateix, l’esforç que esmercem en la reproducció és clarament asimètric, atès que les femelles són les que posseeixen els òrgans i la fisiologia adequats per gestar i alletar les cries. Això genera un fort esbiaix entre ambdós sexes respecte a la possibilitat de realitzar aparellaments diversos.
Tradicionalment, els humans ens hem comportat de forma monògama quant a la cura de la descendència, la qual cosa no exclou que durant l’etapa reproductora una femella es pugui aparellar amb diversos mascles i un mascle amb diverses femelles. Tanmateix, l’esforç que esmercem en la reproducció és clarament asimètric, atès que les femelles són les que posseeixen els òrgans i la fisiologia adequats per gestar i alletar les cries. Això genera un fort esbiaix entre ambdós sexes respecte a la possibilitat de realitzar aparellaments diversos.
Genèticament parlant, la reproducció és l’acte egoista de passar les variants gèniques pròpies a la descendència. En aquest sentit s’ha proposat que, per a les femelles, el fet que el “seu” home s’aparelli amb altres femelles (adulteri masculí) no suposa cap desavantatge quant al manteniment de la seva nissaga genètica, ja que, tenint en compte la tradicional monogàmia quant a la cura dels descendents, el seu home hi continuarà contribuint. En canvi, per al mascle, l’adulteri femení suposa un clar desavantatge quant a l’acte egosita de transmetre els seus gens, atès que haurà de contribuir a alimentar i protegir descendents que no portaran les seves variants gèniques. També hi ha qui diu que les femelles podrien tenir una certa preferència pels mascles adúlters, perquè així els seus descendents també podrien heretar aquesta característica, la qual cosa contribuiria a expandir les variants gèniques de la femella a través dels adulteris dels seus fills.
El color de la pell
La conservació dels fòssils d’Atapuerca
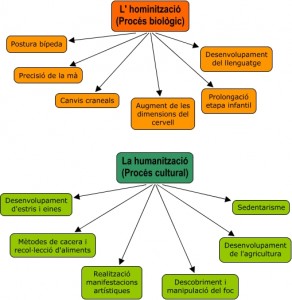
L’arbre evolutiu dels homínids i els fòssils
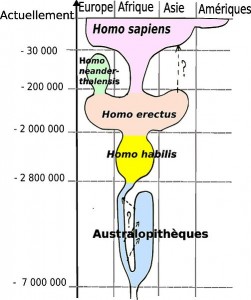
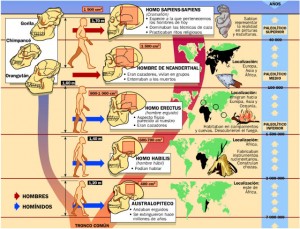
Clicant aquí pots veure un llistat dels diferents fòssils d’homínids trobats.
Un exemple de com la selecció natural també afecta als humans… …i molt !
De nou un text del catedràtic de genètica de la UB David Bueno.
EL DESENVOLUPAMENT TÈCNIC I CULTURAL: UNA NOVA SELECCIÓ NATURAL ?
 Perquè una adaptació quedi reflectida en l’evolució, cal que hi hagi una base genètica prèvia i que la selecció natural l’afavoreixi. En aquest sentit, hi ha constància que el desenvolupament tècnic i cultural ha actuat a manera de selecció natural sobre la nostra pròpia espècie. Un bon exemple n’és la capacitat de pair la llet durant tota la vida, una característica que presenta la meitat de la població humana. L’altra meitat, en canvi, la perd cap als dos anys d’edat.
Perquè una adaptació quedi reflectida en l’evolució, cal que hi hagi una base genètica prèvia i que la selecció natural l’afavoreixi. En aquest sentit, hi ha constància que el desenvolupament tècnic i cultural ha actuat a manera de selecció natural sobre la nostra pròpia espècie. Un bon exemple n’és la capacitat de pair la llet durant tota la vida, una característica que presenta la meitat de la població humana. L’altra meitat, en canvi, la perd cap als dos anys d’edat.
La possibilitat de pair la llet ens la dóna un enzim de l’estómac que la qualla. Per als mamífers, que alletem les cries, és de vital importància per a la supervivència inicial dels descendents. Tanmateix, tots els altres mamífers perden la capacitat de digerir la llet quan se’ls comencen a desenvolupar les dents. Això provoca la fi de l’alletament, i permet que la femella pugui iniciar una nova gestació. En cas contrari, el temps d’alletament podria ser molt més llarg, la qual cosa entraria en conflicte amb l’instint de reproducció de la mare. Per aquest motiu la selecció natural ha afavorit una determinada variant d’aquest gen que es desconnecta a una determinada edat.
Les persones que podem pair la llet tota la vida tenim una variant d’aquest gen que no es desconnecta mai, a causa d’una mutació que va aparèixer fa uns 9.000 anys. Què va passar en aquella època ? Doncs que es va produir un dels salts cientificotècnics i socioculturals més importants de la humanitat, la revolució neolítica, que va permetre que canviéssim l’estil de vida de caçadors-recol·lectors pel d’agricultors i ramaders. I el desenvolupament de la ramaderia ens va proporcionar una font d’aliment molt rica en nutrients essencials: la llet dels animals. Per aquest motiu, aquesta mutació va resultar molt avantatjosa, i la selecció natural la va afavorir.
Tanmateix, si és tan beneficiosa, per què actualment no la tenim totes les persones ? Doncs perquè el mateix desenvolupament cientificotècnic va propiciar que poc després es descobrissin els ferments que quallen la llet i permeten obtenir formatge, iogurt i quèfir. Aquest procés fa la llet més duradora, i també fa innecessària la presència d’enzims a l’estómac, atès que ens permet menjar derivats làctis ja quallats. En conseqüència, aquesta nova descoberta cinetificotècnica va alliberar les persones que no podien pair llet líquida d’aquesta pressió selectiva, i ambdues variants gèniques van perdurar, fins a l’actualitat.
Cap on conduirà el desenvolupament tècnic la nostra evolució ? És que potser hem substituït parcialment la selecció natural sobre la nostra espècie per una selecció, diguem-ne, cientificotècnica ? Afectarà també els nostres instints i, de retruc, la nostra cultura ?